明天就要AP考试了,作为化学部分,大家是否做好准备了呢?老师为大家整理了最新的AP化学知识重难点,在考试前夕,为大家进行详细的讲解。下面让我们一起来看看吧!
Part I:Structure of matter.
这里主要包括atomic structure和bonding,其中后者又包含chemical bond 和intermolecular forces.
在atomic structure部分主要需要掌握electron configuration(electronic structure)以及与其相关的photoelectron spectroscopy(PES)的解析。要注意的是看任何图一定先看清楚坐标轴代表的物理量,PES谱中横坐标代表binding energy,一般从左往右减小,纵坐标代表电子的相对数目,因此对于一个PES全谱(complete PES)从左往右每个峰即对应从低能到高能排列的电子亚层(subshell):1s, 2s, 2p, 3s…
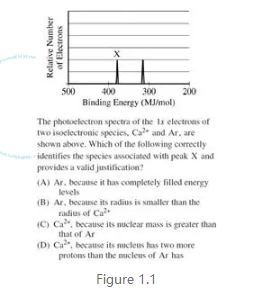
然后按照每层相对电子数目写出谱图代表的物种即可。这里峰位置的相对偏移能显示电子与原子核的作用力强弱,比如在Ca2+和Ar的PES对比谱中前者的1s峰位置要向高能偏移(图1.1),因为在能级相同时(电子所处的位置离原子核距离相近),原子核电荷(nuclear charge)的大小会决定库仑力,从而影响核与电子的结合能。另外,各级电离能与PES谱的对应关系也需要注意,利用电离能的big jump出现的位置确定元素的valence electron也是课堂上强调比较多的考点。另外,原子(离子)未配对电子数的多少与其是否是paramagnetic和magnetic moment的关系也是比较小众的考点。
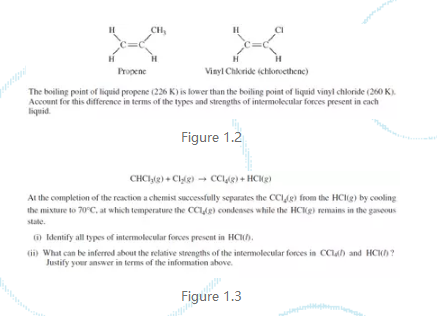
Bonding一节中涉及到的所有作用力都是库仑力,均与电荷多少正相关,与带电粒子之间的距离(一般为半径之和)负相关。该知识点涉及到比较离子化合物lattice energy的大小,离子溶于水之后ion-dipole forces的大小,金属单质中positive core与sea of electrons之间作用力的大小,London dispersion forces的大小(polarizability决定,直接由molar mass体现)和dipole-dipole forces的大小(dipole moment决定,直接由electronegativity差异和molecular geometry估计)。尤其对于两种物质intermolecular forces的大小比较进而决定的boiling point大小比较需要遵循这样一个判断程序:首先判断物质A和B的各自的分子间作用力,London dispersion forces(LDF)是存在任何分子间的,所以两者都会有,然后根据molar mass判断大小,第二步判断是否除此之外有别的力如dipole-dipole forces和hydrogen bonding,当两者的LDF相差很小或者B大于A并且B分子间又有dipole-dipole forces甚至hydrogen bonding,B的boiling point毫无疑问会高于A;若A分子的LDF远高于B,而B分子中又有dipole-dipole forces就需要更多的信息来确定,图1.2和1.3即对应实例。
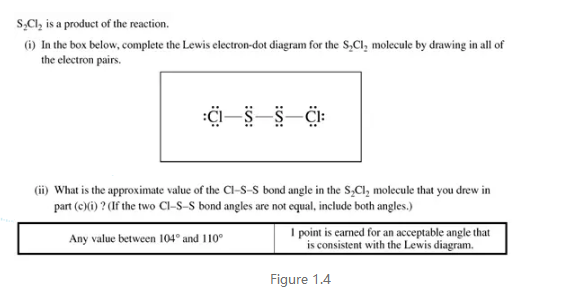
Bonding部分的第二个难点在于分子结构的判断,这部分也是确定分子极性(polarity)进而确定分子间作用力的基础,之所以单独列出来说是基于近几年free response对其考察的力度。从选择题bond length,bond angle的大小比较到free response里直接在Lewis structure基础上判断并给出一个可接受的bond angle,这部分内容重要性可想而知。具体的判断程序在课堂上多次强调和举例说明过,此处需要明确的是关于中心原子周围电子对个数应该包括所有的lone pairs和bonding pairs(其中成键不论bond order只算一对,即单键、双键和三键都算一对电子——其实就是只算bonding pairs里面的sigma bond)。此外derived shape里面键角的确定,一般多一对lone pair会使键角减小2.5度,考试中参考答案都是一个范围,所以建议basic shape(electron domain geometry)为tetrahedral时角度统一为109°,basic shape为trigonal planar时角度统一为118°。
Bonding部分既然都说到Lewis structure了,那么resonance forms的确定以及用formal charge去判断哪种形式更稳定(most likely existed)就需要提一下。在计算完formal charge之后考察哪个结构里面电荷的分配和electronegativity更一致则为更合理的结构,比如有O存在的时候,负电荷更偏向于O则为合理。
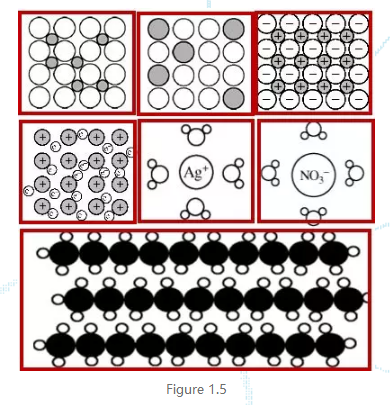
最后值得一提的是,这部分对应的微观放大示意图会比较多,如合金的两种结构(杂原子内嵌型和代替型),离子型固体,金属固体以及分子固体的表示,阴阳离子和水分子的相对位置表示,物质在不同状态、不同温度下分子间距和速率矢量的表示等都需要细心。
来源:葛艳丽 北京新东方北美留学
以上就为大家整理的“2018年5月8日AP化学重难点考前点题一”,更多精彩内容,请关注新东方在线GMAT频道。